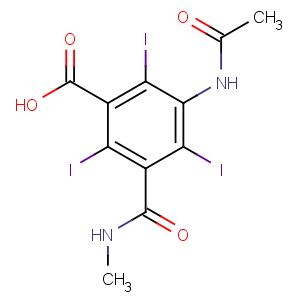
简介
【药品名称】 碘他拉酸
【拼音名】 Diantalasuan
【英文名】 IOTALAMIC ACID
【来源(分子式)与标准】 本品为 5-[(甲氨基)羰基]-3-(乙酰胺基)-2,4 ,6-三碘苯甲酸。
按干燥品计算,含C11H9I3N2O4 不得少于98.5%。
性状
本品为白色结晶性粉末;无臭,无味。
本品在水中或乙醇中微溶,在氯仿中不溶,在氢氧化碱溶液中易溶。 检查 氯化物 取本品0.50g,加水20ml和氨试液数滴,溶解后,滴加硝酸 1.5 ml,搅拌使碘他拉酸析出,滤过,沉淀用少量水洗涤滤液与洗液合并,置50ml纳氏比色 管中,加水使成40ml,依法检查(附录Ⅷ A),与标准氯化钠溶液2.5ml 制成的对照液 比较,不得更浓(0.005%) 。
游离碘 取本品 0.20g,加氢氧化钠试液2.0ml 溶解后,加稀硫酸2.5ml 使析出,放置10分钟,加氯仿5ml ,振摇,氯仿层不得显色。
氨基化合物 取本品1.25g,加水5ml 与氢氧化钠试液5ml 使溶解,加水至100ml ,摇匀,取10ml,加0.1mol/L亚硝酸钠溶液5ml 与盐酸溶液(9→100)10ml,摇匀,放置10 分钟,加2.5 %氨基磺酸铵溶液5ml ,摇匀,放置5 分钟,加碱性β-萘酚试液2ml 与 氢氧化钠试液15ml,加水至50ml,摇匀,照分光光度法(附录Ⅳ A),在485nm 的波长 处测定吸收度,不得过0.25。
干燥失重 取本品,在105 ℃干燥至恒重,减失重量不得过1.0 %(附录Ⅷ L)。
炽灼残渣 取本品1.0g,依法检查(附录Ⅷ N),遗留残渣不得过0.1 %。
重金属 取炽灼残渣项下遗留的残渣,依法检查(附录Ⅷ H第二法),含重金属不 得过百万分之十。
鉴别
(1) 取本品约10mg,置坩埚中,小火加热,即分解产生紫色的碘蒸气。
(2) 本品的红外光吸收图谱应与对照品的图谱(光谱集 678图)一致。
【含量测定】
取本品约0.4g,精密称定,加氢氧化钠试液30ml与锌粉1.0g,加热 回流30分钟,放冷,冷凝管用少量水洗涤,滤过,烧瓶与滤器用水洗涤3 次,每次15ml ,洗液与滤液合并,加冰醋酸5ml 与曙红钠指示液5 滴,用硝酸银滴定液(0.1mol/L)滴 定。每1ml 的硝酸银滴定液(0.1mol/L)相当于20.46mg 的C11H9I3N2O4 。
应用与保存
【类别】 诊断用药。
【贮藏】 遮光,密闭保存。 制剂 碘他拉葡胺注射液
药物分析
方法名称:
碘他拉酸―碘他拉酸的测定―沉淀滴定法
应用范围:
本方法采用沉淀滴定法测定碘他拉酸(C11H9I3N2O4)的含量。
本方法适用于碘他拉酸的测定。
方法原理:
量取本品适量,精密称定,加氢氧化钠试液与锌粉,加热回流,放冷,冷凝管用少量水洗涤,滤过,烧瓶与滤器用水洗涤,洗液与滤液合并,加冰醋酸与曙红钠指示液,用硝酸银滴定液(0.1mol/L)滴定,每1mL硝酸银滴定液(0.1mol/L)相当于20.46mg的C11H9I3N2O4。计算,即得。
试剂:
1. 水(新沸放置至室温)
2. 冰醋酸
3. 曙红钠指示液
4. 氢氧化钠试液
5. 锌粉
6. 硝酸银滴定液(0.1mol/L)
7. 碳酸钙
8. 荧光黄指示液
9. 糊精溶液
10. 基准氯化钠
仪器设备:
试样制备:
1. 曙红钠指示液
取曙红钠0.5g,加水100mL使溶解,即得。
2. 氢氧化钠试液
取氢氧化钠4.3g,加水使溶解成100mL,即得。
3. 硝酸银滴定液(0.1mol/L)
配制:取硝酸银17.5g,加水适量使溶解成1000mL,摇匀。
标定:取在110℃干燥至恒重的基准氯化钠0.2g,精密称定,加水50mL使溶解,再加糊精溶液(1→50)5mL,碳酸钙0.1g与荧光黄指示液8滴,用本液滴定至浑浊液由黄绿色变为紫红色,每1mL硝酸银滴定液(0.1mol/L)相当于5.844mg的氯化钠,根据本液的消耗量与氯化钠的取用量,算出本液的浓度。
4. 荧光黄指示液
取荧光黄0.1g,加乙醇使溶解成100mL。
5. 糊精溶液
取糊精1g,加水使溶解成50mL。
操作步骤:
取本品约0.4g,精密称定,加氢氧化钠试液30mL与锌粉1.0g,加热回流30分钟,放冷,冷凝管用少量水洗涤,滤过,烧瓶与滤器用水洗涤3次,每次15mL,洗液与滤液合并,加冰醋酸5mL与曙红钠指示液5滴,用硝酸银滴定液(0.1mol/L)滴定,每1mL硝酸银滴定液(0.1mol/L)相当于20.46mg的C11H9I3N2O4。
注1:“精密称取”系指称取重量应准确至所称取重量的千分之一,“精密量取”系指量取体积的准确度应符合国家标准中对该体积移液管的精度要求。
注2:“水分测定”用烘干法,取供试品2~5g,平铺于干燥至恒重的扁形称瓶中,厚度不超过5mm,疏松供试品不超过10mm,精密称取,打开瓶盖在100~105℃干燥5小时,将瓶盖盖好,移置干燥器中,冷却30分钟,精密称定重量,再在上述温度干燥1小时,冷却,称重,至连续两次称重的差异不超过5mg为止。根据减失的重量,计算供试品中含水量(%)。
参考文献:
中华人民共和国药典,国家药典委员会编,化学工业出版社,2005年版,二部,p.807。