简介
【药品名称】
通用名称:阿仑膦酸钠片
商用名称:安仑、固邦、福善美 Alendros、Fosamax
英文名称:Alendronate Sodium Tablets
汉语拼音:Alun Linsuanna Pian
【成份】
本品主要成份为:阿仑膦酸钠,
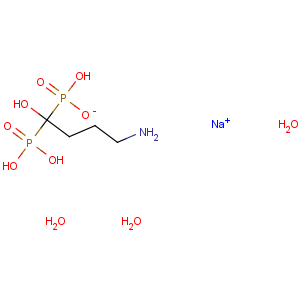
化学名称:(4-氨基-1-羟基亚丁基)二膦酸单钠盐三水合物。
化学结构式:
NH2
│
CH2
│
CH2
│
O CH2 O
? │ ?
HO── P ── C ── P ─ ONa,3H2O
| | |
OH OH OH
分子式:C4H12NNaO7P2?3H2O
分子量:325.12
【性状】本品为白色或类白色片。
规格
70mg(以阿仑膦酸计)
用法用量
本品必须在每天第一次进食、喝饮料或应用其它药物治疗之前的至少半小时,用白水送服,因为其它饮料(包括矿泉水)、食物和一些药物有可能会降低本品的吸收(见[药物相互作用])。
为尽快将药物送至胃部,降低对食道的刺激,本品就在清晨用一满杯白水送服,并且在服药后至少30分种之内和当天第一次进食前,病人应避免躺卧。本品不应在就寝时和清早起床前服用。否则会增加发生食道不良反应的危险(见[注意事项])。
如食物中摄入不足,所有骨质疏松患者都应补充钙和维生素D(见[注意事项])。
老年患者或伴有轻到中度肾功能不全的患者(肌酐清除率35 ~ 60ml/min)不需要调整剂量。因缺乏相关用药经验,对于更严重的肾功能不全患者(肌酐清除率<35ml/min),不推荐使用本品。
绝经后妇女骨质疏松症的治疗:
推荐剂量为:每周1次,1次1片70mg;或每天1次,1次1片10mg;
治疗男性骨质疏松症以增加骨量:
推荐剂量为:每天1次,1次1片10mg。作为一种选择,每周1次,1次1片70mg也可以考虑。
给药说明
1、本品宜于每日首次进食或应用其他药物前至少本小时 ,用温开水200ml(矿泉水等其他饮料、食物和某些药物可能降低本品吸收)。不得咀嚼或吮吸,服药后至少30分钟内及当日进食前,避免躺卧,以免引起食管不良反应(食管炎、食管溃疡和食管糜烂,罕见伴有食管狭窄)。如出现吞咽困难或疼痛、胸骨后疼痛、新发或加重的胃灼热,应停用并做相应处理。
2、开始应用本品前,须先纠正低钙血症。服药期间需补充钙剂。其他矿物质代谢紊乱(例如维生素D缺乏)也应同时治疗。应用糖皮质激素者更需摄入足量的钙和维生素D。
3、口服本品过量可能导致低钙血症、低磷血症和上消化道不良反应,如胃部不适、胃灼热、食管炎、胃炎或溃疡。可服用牛奶或抗酸药以结合阿仑磷酸盐。嘱患者保持直立,以免出现食管刺激现象。
鉴别
(1)取本品约20mg,加水2ml溶解后,加氢氧化钠试液适量使呈碱性,再加茚三酮试液1ml,混合,加热煮沸数分钟,即显紫红色。(2)本品(150℃干燥至恒重)的红外光吸收图谱应与对照品的图谱一致(附录Ⅳ C)。
(3)本品的水溶液显钠盐的鉴别反应(附录Ⅲ)。
检查
酸度 取本品0.8g,加水50ml溶解后,依法测定(附录Ⅵ H),pH值应为4.2~4.6。溶液的澄清度与颜色 取本品0.5g,置50ml量瓶中,加水溶解并稀释至刻度,溶液应澄清无色。
氯化物 取本品1.0g,加水50ml使溶解,分取25ml,依法检查(附录Ⅷ A),与标准氯化钠溶液5.0ml制成的对照液比较,不得更浓(0.01%)。
亚磷酸二氢钠 取本品4.0g,精密称定,置250ml碘量瓶中,加水70ml加热溶解,冷却。加磷酸盐缓冲液(取磷酸二氢钠6.9g,加水500ml溶解后,加0.1mol/L氢氧化钠溶液400ml,摇匀)20ml,用氢氧化钠溶液(1:4)调节pH值7.3±0.2,精密加入碘滴定液(0.005mol/L)50ml,摇匀,密塞,避光放置3小时,用6mol/L醋酸溶液调节pH值4.5±0.2,用硫代硫酸钠滴定液(0.01mol/L)滴定,至近终点时,加入淀粉指示液2ml,继续滴定至蓝色消失,并将滴定结果用空白试验校正,每1ml碘滴定液(0.005mol/L)相当于0.5199mg的NaH2PO3,计算亚磷酸二氢钠NaH2PO3不得过0.3%。
有关物质 照高效液相色谱法(附录Ⅴ D)测定。
色谱条件与系统适用性试验 用苯乙烯基-二乙基苯共聚物为填充剂(参考色谱柱:Polymer Laboratories生产的 PLRP-S柱);以缓冲液(取枸橼酸钠2.94g和磷酸氢二钠1.42g,加水至1000ml,用磷酸调节pH值至8.0)-乙腈(85:15)为流动相A,缓冲液-乙腈(30:70)为流动相B,按下表进行梯度洗脱;检测波长为266nm;柱温45℃。精密量取对照溶液、灵敏度试验溶液各20μl,注入液相色谱仪中,调节仪器灵敏度,使对照溶液色谱图中主成分峰的峰高为满量程的约10%~20%, 灵敏度试验溶液色谱图中应检出阿仑膦酸钠峰。
| 时间(分钟) | 流动相A% | 流动相B% |
| 0 | 100 | 0 |
| 15 | 50 | 50 |
| 25 | 0 | 100 |
| 27 | 100 | 0 |
| 37 | 100 | 0 |
供试品溶液的制备 取本品约30mg,精密称定,置50ml量瓶中,用0.1mol/L枸橼酸钠溶液溶解并稀释至刻度,摇匀,即得供试品贮备溶液。精密量取供试品贮备溶液5ml,置50ml具塞的离心管中,分别精密加入0.05mol/L硼砂溶液、乙腈各5.0ml,在涡流旋转器上混合20秒,再精密加入0.4%的氯甲酸芴甲酯乙腈溶液5.0ml,涡流混合45秒后,置45℃水浴中,放置30分钟,再加入二氯甲烷20ml,涡流混合60秒,离心(1500转/分),取上层清液,即得。
对照溶液的制备 精密量取上述供试品溶液1ml,置100ml量瓶中,以溶剂[0.1mol/L枸橼酸钠溶液和0.05mol/L硼砂溶液(1:1)的混合液]稀释至刻度,摇匀,精密量取10ml,置100ml量瓶中,以溶剂[0.1mol/L枸橼酸钠溶液和0.05mol/L硼砂溶液(1:1)的混合液]稀释至刻度,摇匀,即得。
灵敏度试验溶液的制备 精密量取上述对照溶液5ml,置10ml量瓶中,以溶剂[0.1mol/L枸橼酸钠溶液和0.05mol/L硼砂溶液(1:1)的混合液]稀释至刻度,摇匀,即得。
空白溶剂的配制 精密量取0.1mol/L枸橼酸钠溶液5.0ml,同供试品溶液制备项下“置50ml具塞的离心管中…取上层清液”操作,即得。
测定法 精密量取供试品溶液及对照溶液各20μl,注入液相色谱仪中,记录色谱图至主成分峰保留时间的5倍。供试品溶液色谱图中如有杂质峰(峰面积小于灵敏度试验溶液色谱图中阿仑膦酸钠峰面积的单个杂质峰及空白溶剂峰不计),单个杂质的峰面积不得过对照溶液主峰面积(0.1%),各杂质峰面积的和不得过对照溶液主峰面积的5倍(0.5%)。
干燥失重 取本品1.0g,在150℃干燥至恒重,减失重量应为16.0%~17.5%(附录Ⅷ L)。
重金属 取本品1.0g,依法检查(附录Ⅷ H 第三法),含重金属不得过百万分之十。
含量测定
取本品约0.6g,精密称定,加新沸过的冷水75ml,温热溶解,放冷,照电位滴定法(附录Ⅶ A),用氢氧化钠滴定液(0.1mol/L)滴定。每1ml的氢氧化钠滴定液(0.1mol/L)相当于27.11mg的C4H12NNaO7P2。
类别
抗骨质疏松药。注:氯甲酸芴甲酯(9-fluorenylmethy chloroformate),缩写为FMOC。
不良反应
据国外文献报道:
临床研究
在临床研究中,本品一般耐受性良好。在一些长达5年的研究中,不良反应通常是轻微的,一般不需要停止治疗。
治疗绝经后妇女骨质疏松症
两个(美国和多国)大型、实际上设计完全相同的为期三年、安慰剂对照、双肓、多中心研究中,每天应用本品10mg,结果显示总的安全性情况与安慰剂组相似。研究者所报告的在≥1%的每天接受本品10mg的病人中,所发生的可能、很可能或一定和药物相关且发生率高于安慰剂组的消化不良反应包括;腹痛(本品6.6%,安慰剂4.8%)、消化不良(3.6%,3.5%)、食管溃疡(1.5%,0.0%)、吞咽困难(1.0%,0.0%)和腹胀(1.0%,0.8%)
皮疹和红斑很少发生。
另外,研究者所报告的在≥1%的每天接受本品10mg治疗的病人,发生的可能、很可能或一定与药物相关的,而且发生率高于安慰剂组的不良反应有:肌肉骨骼疼痛(本品4.1%,安慰剂2.5%)、便秘(3.1%,1.8%)、腹泻(3.1%,1.8%)、胀气(2.6%,0.5%)和头痛(2.6%,1.5%)。
在以上研究的两年延长期(治疗4年和5年的)中,本品10mg/天的总体安全状况与安慰剂组对照的3年期间所观察到的相似。另外,由于任何不良反应而停用本品每天10mg的患者比例也与该研究的前3年相似。
以下是研究者报告可能、很可能或一定与药物有关的不良事件,其发生于为期一年临床中任一组≥1%的病人中,或发生于为期三年临床中≥1%的接受每天阿仑膦酸钠10mg的病人且发生率高于安慰剂组。
| 一年临床 | 三年临床 |
| 阿仑膦酸钠每周
70mg组(n=519)% | 阿仑膦酸钠每天
10mg组(n=370)% | 阿仑膦酸钠每天
10mg组(n=196)% | 安慰剂组
(n=397)% |
| 胃肠道 |
|
|
|
|
| 腹痛 | 3.7 | 3.0 | 6.6 | 4.8 |
| 消化不良 | 2.7 | 2.2 | 3.6 | 3.5 |
| 返酸 | 1.9 | 2.4 | 2.0 | 4.3 |
| 恶心 | 1.9 | 2.4 | 3.6 | 4.0 |
| 腹胀 | 1.0 | 1.4 | 1.0 | 0.8 |
| 便秘 | 0.8 | 1.6 | 3.1 | 1.8 |
| 腹泻 | 0.6 | 0.5 | 3.1 | 1.8 |
| 吞咽困难 | 0.4 | 0.5 | 1.0 | 0.0 |
| 肠胀气 | 0.4 | 1.6 | 2.6 | 0.5 |
| 胃炎 | 0.2 | 1.1 | 0.5 | 1.3 |
| 胃溃疡 | 0.0 | 1.1 | 0.0 | 0.0 |
| 食管溃疡 | 0.0 | 0.0 | 1.5 | 0.0 |
| 骨肉骨骼 |
|
|
|
|
骨肉骨骼
(骨、肌肉或关节)痛 |
2.9 |
3.2 |
4.1 |
2.5 |
| 肌肉痉挛 | 0.2 | 1.1 | 0.0 | 1.0 |
| 神经系统 |
|
|
|
|
| 头痛 | 0.4 | 0.3 | 2.6 | 1.5 |
治疗男性骨质疏松症
在一项为期两年疗程的双肓、安慰剂对照、多中心的临床研究中,146名每日服用本品10mg的男性患者的安全性资料与绝经后妇女的一致。
其它研究
一项十周的内窥镜研究(包括男女性227人,平均年龄55岁)发现,本品每周一次70mg的治疗组与安慰剂组在引起上消化道病变方面没有差别。
另一项为期一年的研究(包括男女性335人,平均年龄50岁)发现,本品每周一次70mg的治疗组与安慰剂组在总的安全性与耐受性方面相似,并且,男女之间没有差别。
产品上市后经验
药品上市应用后已报告的不良反应如下:
全身反应:过敏反应,包括荨麻疹和罕见的血管性水肿。同其他二膦酸盐一样,在开始服用本品时,会发生一过性的急性期反应(肌痛、不适和罕见发烧)。在存在诱因条件时,会发生罕见的低钙血症。
胃肠道反应:恶心、呕吐、食管炎、食道糜烂、食道溃疡、罕见食管狭窄或穿孔、口咽溃疡。某些较为严重并伴有并发症,尽管它们与药物的因果关系尚未确定(见[注意事项]及[用法用量])。在拔牙和/或局部感染愈合延迟时,会发生罕见的下颌局部骨坏死。
肌肉骨骼:骨、关节、和/或肌肉疼痛,罕见严重和/或致残的情况。
皮肤:皮疹(偶拌有对光过敏),搔痒。罕见的严重皮肤反应,包括Stevens-Johnson综合征和毒性表皮坏死松懈。
特殊感觉:罕见眼色素层炎,罕见虹膜炎或虹膜外表层炎。
实验室结果
在双肓、多中心、安慰剂对照的临床研究中,本品组分别有18%和10%的病人发生无症状性、轻微且短暂的血清钙和血清磷的下降,安慰剂组中分别有12%和3%。但是血清钙<8.0mg/dL(2.0mmol/L)和血清磷≤2.0mg/dL(0.65mmol/L)的发生率,两组情况相似。
禁忌
◆ 导致食管排空延迟的食管异物,例如狭窄或迟缓不能
◆ 不能站立或坐直30分钟者
◆ 对本品任何成分过敏者
◆ 低钙血症者(见[注意事项])
注意事项
和其它二膦酸盐一样,本品可能对上消化道粘膜产生局部刺激。
在服用本品的病人中,已报告的食管不良反应有食管炎、食管溃疡和食管糜烂,罕有食管狭窄和穿孔的报告。其中有些病例,因这些不良反应严重而需要住院治疗。因此,医生应该警惕可能发生食管反应的任何症状和体征,应指导病人如出现吞咽困难、吞咽痛、胸骨后疼痛或新发胃灼热或胃灼热加重,停用本品并就医。
在服用本品后躺卧、和/或不用一满怀水送服药物、和/或出现提示食管刺激的症状后仍继续服药的病人,发生严重食管不良反应的危险性较大。因此,提供病人详尽的用药指导,让其充分理解是很重要的(见[用法与用量])。
尽管在广泛的临床试验中未观察到胃和十二指肠溃疡的增加,上市后却有极少量的报告,某些极为严重的并伴有并发症。然而,它们与药物的因果关系尚未确定。
因为本品对上消化道粘膜有刺激性作用并有可能加重潜在的疾病,故应慎用于患有活动性上消化道疾病如吞咽困难、食管疾病、胃炎、十二指肠炎、溃疡或最近有胃肠道病史(近1年内),如消化道溃疡或活动性胃肠道出血或消化道手术(除外幽门成形术)的病人。
为了便于将本品送至胃部并降低对食管的刺激,应指导病人用一满杯水吞服药物,并且至少在30分钟内及在当天第一次进食之前不要躺卧。病人不应该咀嚼或吮吸药片,以防口咽部溃疡。应该特别指导病人在就寝前和清早起床前不要服用本品。应该告诉病人,若不遵医嘱就可能增加出食管问题的危险性。应该告诉病人,如果发生食管疾病的症状(如吞咽困难或疼痛、胸骨后疼痛或新发胃灼热或胃灼热加重),应该停用本品并请医生诊断治疗。
服用二膦酸盐的病人会发生骨、关节和/或肌肉疼痛。在上市后经验总结中,这些症状严重和/或致残的情况是罕见的(见不良反应,上市后经验)。症状发作的时间从开始治疗后一天至几个月不等。多数病人停药后症状缓解。当再服用同样的药物或再服用另一种二膦酸盐时,症状会再次出现。
应当告诉病人,如果漏服了一次每周剂量,应当在记起后的早晨服用一片。不可以在同一天服用两片,而应按其最初选择的日期计划,仍然每周服用一片。
肌酐清除率<35ml/min的病人,不推荐应用本品(见[用法与用量])
除雌激素缺乏和老龄之外,还应考虑其他造成骨质疏松的原因。
在开始应用本品治疗之前,必须先纠正低钙血症(见[禁忌])。
其它影响矿物代谢的异常(例如维生素D缺乏),也应该得到有效治疗。由于阿仑膦酸钠可增加骨密度,因此可出现轻度的、无症状的血钙和磷酸盐下降,特别是使用糖皮质激素治疗的患者,可能他们的钙吸收减少。因此,使用糖皮质激素的患者保证足够的钙和维生素D是很重要的。
孕妇及哺乳期妇女用药
未在孕妇中做过研究,孕妇不宜使用。
未在哺乳期妇女中做过研究,不应用于这类病人。
儿童用药
未在儿童中做过研究,儿童不宜使用。
老年用药
在临床研究中,未发现本品有年龄相关性的疗效和安全性方面的差异,或遵医嘱。
药物的相互作用
如果同时服用钙补充制剂、抗酸药物和其它口服药物可能会干扰本品吸收。因此,病人在服用本品以后,必须等待半小时后,才可服用其他药物。
预计无其它具有临床意义的药物相互作用。
两项为期一年或两年临床研究对绝经后骨质疏松妇女同时应用激素替代治疗(雌激素±孕激素)(静脉同时经皮给药或口服给药)和本品进行了评价。与单独应用相比,联合应用激素替代治疗和本品能更多地增加骨量,更多地降低骨转换。在这些研究中,联合治疗与单独治疗在安全性和可耐受性方面是一致的。
特异性相互作用研究尚未进行。在治疗男性和绝经后妇女的骨质疏松症的研究中,本品已与各种常用处方药同时使用,无明显确定的临床不良相互作用。
药物过量
目前尚没有本品过量用药的资料。口服药物过量可能会导致低钙血症、低磷血症和上消化道不良事件,如胃部不适、胃灼热、食管炎、胃炎或溃疡。应给于牛奶或抗酸剂以结合阿仑膦酸钠。由于食管刺激的危险,不应该诱导呕吐,病人应保持直立。
药理作用
据国外文献报道:
作用机制
动物研究发现本品有下述作用方式。在细胞水平,阿仑膦酸钠对骨吸收部位特别是破骨细胞作用的部位有亲嗜性。正常情况下,破骨细胞粘附于骨表面但并不粗糙,而粗糙的边缘则是骨吸收活跃的标志。阿仑膦酸钠不影响破骨细胞的聚集或粘附,但它确实能够抑制破骨细胞的活性。小鼠体内进行的有关标记有放射性活性的[3H]阿仑膦酸钠在骨内作用部位的研究显示,破骨细胞表面的摄入是成骨细胞表面的10倍。标记有放射活性[3H]阿仑膦酸钠分别给予大鼠6天和小鼠49天后,检查其骨组织发现,正常骨形成于阿仑膦酸钠上面,后者与基质结合后不再具有药理活性,因此阿仑膦酸钠必须持续服用以抑制新形成的吸收表面的破骨细胞。狒狒和大鼠的组织形态测量学显示,阿仑膦酸钠能降低骨转换(即,骨重建部位的数量),而且在这些重建部位,骨形成超过骨吸收,从而使骨量增加。
动物毒理
急性毒性
对雌性大鼠和小鼠来说,口服阿仑膦酸钠的LD50值分别为552mg/kg(3256mg/m2)和966mg/kg(2898mg/m2)(相当于人类口服剂量*27600和48300mg)。对雌性鼠,这些值要略高一些,分别为626mg/kg和1280mg/kg。而狗口服剂量达200mg/kg(4000mg/m2)仍未见致死作用(相当于人类口服剂量*10000mg)。
*以患者的体重为50公斤计。
慢性毒性
对大鼠和狗分别进行的长达1年的和3年的重复剂量 ― 毒性研究发现,阿仑膦酸钠的相关变化有以下几个方面:在内源性软骨骨形成区保留了最初的松质骨;碱性磷酸酶活性持续下降;血钙和血磷的浓度一过性下降。这些都与阿仑膦酸钠预期的药理活性有关。对肾毒性最敏感的物种(如狗)出现肾毒性的剂量相当于人类至少应用100mg。大鼠需要更高的剂量才表现出这种肾毒性。胃肠毒性只出现在啮齿动物。这可能是由于对黏膜的直接作用,且仅发生在剂量超过2.5mg/kg/天时。
致癌作用
口服给予大鼠阿仑膦酸钠每天3.75mg/kg观察105周以及口服给予小鼠阿仑膦酸钠10mg/kg/天观察92周,均未发现有致癌作用。
致突变作用
无论有无代谢活性,体外微生物致突变试验未发现阿仑膦酸钠有致突变的作用。同样,体外哺乳细胞致突变试验、体外大鼠肝细胞碱性洗脱试验以及静脉给予小鼠阿仑膦酸钠每天25mg/kg(75mg/m2)体内染色体畸变试验也均未发现其有致突变作用。但是,中国仓鼠卵细胞的体外染色体畸变试验发现:阿仑膦酸钠浓度大于5mM时有弱细胞毒作用,这对人类来说无相关性。因为,体内的治疗剂量不可能达到同样的浓度。而且,五项基因毒性研究中有四项都是纯阴性结果,包括与人类致癌可能性最直接相关的研究(体内染色体畸变试验和微生物致突变试验),以及大鼠和小鼠体内的致癌研究阴性结果均表明阿仑膦酸钠对人类没有基因毒性和致癌的危险。
繁殖
口服给予大鼠阿仑膦酸钠每天5mg/kg对两性的生育和繁殖能力都没有影响。这些研究中发现的唯一与药物相关的影响是大鼠分娩困难。这与药物介导的低钙血症直接相关,这种影响可通过给大鼠补充钙来预防。而且,每天1.25mg/kg的剂量没有任何影响。
生长发育
有关生长发育的毒性研究中,给予大鼠阿仑膦酸钠每天25mg/kg和给予兔子每天35mg/kg均未发现有不良影响。
药代动力学
据国外文献报道:
吸收
以静脉剂量作参考,空腹有标准早餐前2小时给予阿仑膦酸钠5 - 70mg,其平均口服生物利用度在女性为0.64%,在男性口服10mg为0.6%,两者相似。如果在标准早餐前1或1.5小时给药,其生物利用度在两性有类似下降(约40%)。骨质疏松研究证明,在每天第一次进食或喝饮料前至少30分钟给予本品才发挥作用。
如果在标准早餐后2小时以上给药,其生物利用度可以忽略不计。阿仑膦酸钠与咖啡或桔汁同服可使其生物利用度下降约60% 。
对健康者来说,口服给予泼尼松(20mg每天三次,连用5天)对阿仑膦酸钠的口服生物利用度的影响没有临床意义(平均增加20 - 44%)。
分布
研究表明,静脉给予大鼠阿仑膦酸钠1mg/kg后,其瞬间分布于软组织,但接着迅速再分布于骨组织或通过尿排泄。其在人体内的平均稳态分布容积,除了骨组织外,至少为28L。口服给予治疗剂量的阿仑膦酸钠由于其在血浆内的浓度过低,难以进行检验分析(小于5ng/ml)。其血浆蛋白结合率为78% 。
代谢
还没有证据表明阿仑膦酸钠在动物或人体内代谢。
清除
一次性静脉给予C14标记的阿仑膦酸钠发现,约50%的放射性活性在72小时内由尿排泄,粪便中没有或只有很少量的放射活性。一次性静脉给予10mg阿仑膦酸钠后测定其肾清除率为71ml/min,全身清除率不超过200ml/min。静脉给药后6小时内其血浆浓度下降95%以上。其在人体内的终末半衰期估计大于10年,这提示阿仑膦酸钠从骨骼中释放。
病人特征
临床前研究表明此药不在骨内沉积而迅速由尿排泄。在动物身上长期积累静脉给药35ml/kg没有发现骨吸收饱和的证据。尽管还没有临床资料,但肾功能受损时,和动物研究的结果一样,阿仑膦酸钠通过肾的清除很可能会下降。因此,当肾功能受损时,阿仑膦酸钠在体内的蓄积可能会增加(见[用法用量])。
贮藏
密闭保存。
发展历史
骨质疏松症是一个世界范围的、越来越引起人们重视的健康问题。目前全世界约2亿人患有骨质疏松,其发病率已跃居常见病、多发病的第七位。当前,我国已进入老龄社会,老年病尤其是骨质疏松症的防治成为重要的研究课题。老年性骨质疏松症是老年人,尤其是绝经期后妇女的常见病、多发病。因此对于骨质疏松治疗的药物也引起关注与重视。
现有的防治老年性骨质疏松的药物基本上有两大类,即降钙素类药物和雌性激素类药物。降钙素价格昂贵,在国内难以推广;长期使用雌性激素有一定的副作用,且雌性激素不能使丢失的骨组织恢复。二膦酸盐类药物是近二十年发展起来的一类新药,对老年性骨质疏松的防治在国外已引起重视,其用于临床有如下特点:①不仅能抑制骨吸收,还能增加骨量,使丧失的骨组织恢复;②能促进骨小梁的重建,也能减少吸收陷窝深度;③短期用药,长期显效。另外,双膦酸盐还是恶性肿瘤及佩吉特骨病引起的高钙血症的一线治疗药物。
阿仑膦酸钠由意大利Instituto Gentili公司创制,1993年在意大利以商品名Alendros上市,1995年美国以Fosamax的名称上市,用于治疗骨质疏松症和变形性骨炎,1997年5月FDA再次批准其预防骨质疏松和预防骨折的扩大适应症,成为第一个被FDA批准用于预防骨质疏松症的非激素类药物,阿仑膦酸钠对骨的增重作用类似于雌激素,优于降钙素,能显著增加骨密度,降低骨折发生率,口服有效,作用持久,具有良好的耐受性和较高的安全性。
双膦酸盐中的阿仑膦酸钠是在全球市场表现不错的产品之一,1999年销售额突破10亿美元后,业绩平稳上升,2000年FDA批准追加治疗男性老年骨质疏松症,又推动产品的升温。2002年福善美在全球畅销药品中的排名进入18位,销售额为22.5亿美元。2005年的全球销售额达32亿美元。本品在国际由于专利即将到期,会继续增长,但分额会减少,但在国内属于增长期的品种,应该有很好利润空间。
生产厂家
生产企业众多,可上国家食品药品监督管理局网站查询。
原料
阿仑膦酸钠
Cas No: 121268-17-5
分子式: C4H12NNaO7P2.3(H2O)
分子量: 325.12
性状:白色至类白色结晶性粉末
含量:98.0~102.0%
用途: 抗骨质疏松药